И все же сама идея, что нервные клетки используют АТФ в качестве нейромедиатора, вызывала сомнения. Только в 1990-х гг. появились молекулярные методы, с помощью которых сразу в нескольких лабораториях были идентифицированы рецепторы АТФ, что сразу позволило исследовать все многообразие действий, оказываемых этой молекулой на нервные и другие клетки.
Как показали дальнейшие исследования, механизм действия двух типов рецепторов существенно различается. Р2Х-рецепторы относятся к суперсемейству ионных каналов, открываемых нейтромедиаторами. Один из нас (Как) совместно с другими исследователями обнаружил, что, связываясь с АТФ, Р2Х-рецепторы «открываются» в буквальном смысле этого слова и образуют трансмембранный канал, по которому в клетку устремляются натриевые и кальциевые ионы. В отличие от этого рецепторы Р2Y при связывании с АТФ запускают в клетке каскад межмолекулярных взаимодействий, в результате которых в цитоплазму высвобождаются внутриклеточные запасы кальция.
И в том, и в другом случае кальций может повлиять на другие события на молекулярном уровне и изменить поведение клетки.
Молекула АТФ находится в синаптической щели совсем не долго, но ее влияние на активацию рецептора в одних случаях оказывается кратковременным, порядка миллисекунд, а в других длится годами. Например, резкий приток в клетку ионов кальция через Р2Х-каналы может привести к секреции последней других нейромедиаторов (что наблюдалось в тканях мозга),а высвобождение этих же ионов из внутриклеточных депо в результате активации P2Y может повлиять на активность генов, опосредующих пролиферацию клеток, и привести к изменениям в тканях, имеющим долговременные последствия.
Механизм действия АТФ как сигнальной молекулы представляется еще более сложным, когда в дело вступают другие внеклеточные системы сигнализации. Известно, например, что обширное семейство ферментов под названием экто-АТФазы, находящихся на поверхности большинства клеток, быстро отщепляют от молекулы АТФ фосфатные группы, превращая АТФ сначала в аденозиндифосфат (АДФ), затем в аденозинмонофосфат (АМФ), и наконец в аденозин. Каждый из продуктов расщепления АТФ может действовать на клетку по-своему.
Совместное влияние на клетку оказывают не только АТФ и продукты его расщепления; в нервной системе у АТФ есть и другие партнеры, в отношении которых он действует как конейромедиатор. Такое явление, обнаруженное Бернстоком еще в 1976 г., помогло опровергнуть устоявшееся мнение, что любой нейрон синтезирует, запасает и вы-
ВИДЫ РЕЦЕПТОРОВ
Известны два вида рецепторов АТФ. Ре-
цепторы Р2Х — это кальциевые и натри
евые ионные каналы, открывающиеся
в ответ на связывание АТФ с их внекле
точной частью. Когда молекула АТФ при
соединяется к рецептору Р2Y, запускает
ся каскад внутриклеточных сигнальных
процессов, в результате чего ионы каль
ция высвобождаются из внутриклеточ
ных депо в цитоплазму. В обоих случаях
повышение концентрации ионов кальция
в клетке может привести в частности
к кратковременному сокращению мышц.
Активация Р2Y может инициировать раз
ного рода межмолекулярные взаимо
действия и изменение генной активности,
что вызывает долговременные эффекты,
например клеточную пролиферацию
свобождает всего один тип нейромедиаторов. Накоплено множество свидетельств в пользу того, что АТР
обычно высвобождается совместно с такими нейромедиаторами, как всем известные норадреналин
и ацетилхолин. Впервые концепция конейромедиатора была выдвинута относительно АТФ. Сегодня известны и другие примеры подобного партнерства: ГАМК и глицин, дофамин и серотонин, ацетилхолин
и глутамат. Мы имеем здесь еще один пример того, как исследование сигнальных функций АТФ по
могло выявить более универсальные физиологические закономерности и наметить новые направления развития других областей.
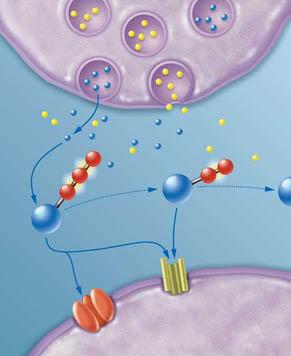
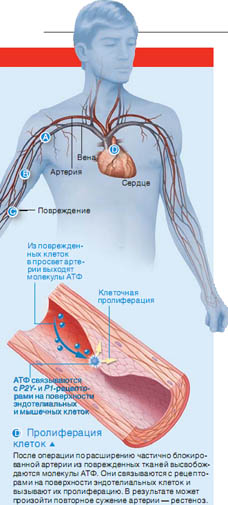
Увеличение тока крови вызывает сдвиг
эндотелиальных клеток, выстилающих
стенки кровеносного сосуда; в резуль
тате из клеток высвобождаются
молекулы АТФ, которые активируют
рецепторы ближайших клеток. В ответ
они секретируют оксид азота, который
способствует расширению сосуда
Роль АТФ в поддержании
нормы и борьбе с патологиями
После всего, что мы узнали об АТФ, нас не должно удивлять участие этой молекулы в функционировании всех пяти органов чувств. Так, показано, что рецепторы АТФ на поверхности нервных клеток в сетчатке глаза реагируют на информацию, поступающую от палочек и колбочек (клеток, воспринимающих световые сигналы). В свою очередь, нервные клетки сетчатки используют
АТФ и ацетилхолин в качестве конейромедиаторов для передачи информации в центры головного мозга, отвечающие за ее обработку. Помимо повседневной работы АТФ, по данным нескольких групп ученых, участвует как сигнальная молекула в очень важном акте в процессе развития эмбриона — формировании зрительной системы. Николас Дейл (Nicholas Dale) из Уорикского университета в Англии вместе со своими коллегами показал, что высвобождение АТФ в строго определенный момент развития эмбриона действительно служит сигналом к началу формирования глаза.
Такую же роль он играет в развитии улитки внутреннего уха — структуры, ответственной за восприятие звука. АТФ участвует в работе слухового аппарата и у взрослого человека. Полость улитки выстилают до 50 тыс. волосковых сенсорных клеток, и примерно половина из них имеют АТФ-рецепторы, которые, как было показано, в ряде случаев опосредуют импульсацию нейронов. Далее, вкусовые сосочки на кончике языка несут Р2Х-рецепторы, опосредующие вкусовые
ощущения. Сью Киннамон (Sue C. Kinnamon) и ее коллеги из Университета штата Колорадо в ходе хорошо продуманных и организованных экспериментов продемонстрировали, что АТФ представляет собой жизненно важный нейромедиатор, передающий сигналы от вкусовых сосочков соответствующим нервным клеткам, и что мыши, лишенные Р2Х2
- и Р2Х3-рецепторов, не способны к восприятию вкуса.
Интересно, что такие же рецепторы опосредуют некоторые болевые ощущения. Многие знают не понаслышке, что подкожные инъекции АТФ весьма болезненны. Недавно группа физиологов из Школы медицины, стоматологии и биомедицинских наук при Королевском колледже в Лондоне показала, что боль возникает в результате активации Р2Х-рецепторов в нервных
окончаниях в коже, опосредующих тактильные и болевые ощущения. Связь АТФ с другим видом боли, а именно возникающей при повреждении нервов, имеет иной характер. Эксперименты, проведенные Кадзухиде Иноуе (Kazuhide Inoue) из Университета Кюсю в Японии и Майклом Салтером (Michael Salter) из Университета Торонто свидетельствуют, что в этом случае происходит активация АТФ-рецепторов на поверхности клеток микроглии в спинном мозге. Микроглия в свою
очередь секретирует молекулы, которые раздражают нервные волокна, что и вызывает хроническую боль (см.: Филдс Д. Новые подозреваемые по делу о хронической боли //ВМН, № 1, 2010).
Уже сейчас некоторые фармацевтические компании намереваются использовать Р2Х-рецепторы в качестве мишеней для новых лекарственных средств при неврологических болях и болях, сопровождающих воспаление. И это только одна
из возможных областей применения АТФ или их рецепторов в медицинских целях. В том же ряду находятся сердечно-сосудистые заболевания. Чтобы понять причину, нужно проследить, что происходит при таких патологиях. Клетки, получившие физические повреждения или неправильно функционирующие, могут высвобождать АТФ в межклеточную среду. Часто это служит сигналом для организма к включению механизмов репарации, в частности к выработке в повышенных количествах тромбоцитов и образованию сгустков крови, останавливающих кровотечение. У тромбоцитов имеются рецепторы подтипа P2Y12; их активация внеклеточными молекулами АТФ и вызывает такие изменения в клетках, которые ускоряют образование сгустков. Эти же события лежат в основе возникновения тромбов в кровеносных сосудах, что может привести к инфаркту или инсульту. Уже создано лекарство-«блокбастер» под названием клопидогрел, которое блокирует рецепторы P2Y12 и тем самым предо
|
| ОБ АВТОРАХ
Джеффри Бернсток (Geoffrey Burnstock) в течение 22 лет заведовал кафедрой
на факультете анатомии и биологии развития Юниверсити-колледжа Лондонского
университета. В 1972 г. высказал предположение, что молекулы АТФ играют роль
переносчиков информации в организме. В настоящее время — президент Центра
по изучению вегетативной нервной системы при Медицинской школе Университетс
кого колледжа Лондонского университета. Удостоен многочисленных наград и пре
мий. Балджит Как (Baljit S. Khakh) — физиолог и нейробиолог, доцент Медицинской
школы им. Дэвида Геффена при Калифорнийском университете в Лос-Анджелесе.
Занимается созданием искусственных рецепторов; в частности, им разработан
АТФ-рецептор, с помощью которого можно исследовать реакцию клеток на АТФ. |
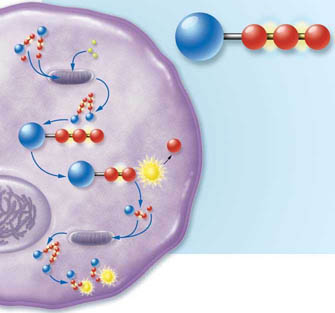
АНАТОМИЯ АТФ
В качестве нейромедиатора АТФ
непосредственно участвуют
в функционировании головного моз
га и сенсорных рецепторов, а также
в регуляции работы мышц и других
органов и тканей. Высвобождаясь из
клеток, не относящихся к нервной
системе, АТФ часто служит «спуско
вым крючком» для защитных реак
ций. Ниже приведены некоторые
примеры действия АТФ на различ
ные органы и ткани. В одних случаях
эти функции уже установлены, в дру
гих изучаются
МОЗГ. АТФ опосредует связь между ней
ронами, а также между нейронами и клет
ками глии. Информация, переносимая
этими молекулами и продуктом их рас
щепления аденозином, влияет на сон, па
мять, обучаемость, двигательную актив
ность. А если сигнал слишком сильный,
может развиться эпилепсия или другие
психические расстройства. АТФ способс
твует заживлению ран, но в то же время
может запускать процесс апоптоза при
нейродегенеративных заболеваниях
СЕНСОРНЫЕ ОРГАНЫ И БОЛЕВЫЕ
ОЩУЩЕНИЯ.
АТФ регулирует, а в неко
торых случаях переносит информацию
от сенсорных нервов глаз, ушей, носа
и языка в головной мозг. Участвует в пере
даче в головной мозг болевых стимулов
СЕРДЦЕ. Молекулы АТФ, высвобождае
мые вместе с норадреналином нервны
ми клетками вегетативной нервной сис
темы, стимулируют сокращения сердеч
ной мышцы. Нарушения в работе этой
сигнальной системы вызывают аритмию
и изменение артериального давления
ДРУГИЕ ОРГАНЫ. АТФ, высвобождае
мый нервными клетками кишечника,
способствует сокращению его стенок
и секреции пищеварительных фермен
тов. АТФ участвует также в регуляции
эрекции, сокращений стенок мочевого
пузыря
КОСТНАЯ ТКАНЬ. Активация АТФ-ре
цепторов стимулирует процессы восста
новления костной ткани и подавляет про
цессы ее разрушения
КОЖА. Активация АТФ-рецепторов спо
собствует заживлению ран, а также, воз
можно, участвует в нормализации
процессов клеточной пролиферации
при таких заболеваниях, как псориаз
и склеродермия
ИММУННАЯ СИСТЕМА. Молекулы АТФ,
выходящие из клеток при повреждениях
тканей, стимулируют клетки иммунной
системы к запуску воспаления — защит
ной реакции организма. Однако слиш
ком сильное и длительное воспаление
может привести к нежелательным пос
ледствиям, например ревматоидному
артриту. АТФ в качестве переносчика ин
формации помогает клеткам иммунной
системы уничтожать клетки, инфициро
ванные патогенными бактериями
твращает стимулирующее действие АТФ, а несколько сходных препара тов проходят последние стадии клинических испытаний.
Еще одно поле деятельности для терапии, нацеленной на АТФ, — пищеварительная система. Джеймс Галлиган (James J. Galligan) и другие сотрудники Университета штата Мичиган показали, что АТФ, высвобождаемый из нервных клеток
кишечника, связывается с Р2Х- и P2Y-рецепторами стенок и участвует в регуляции их ритмичных сокращений, проталкивающих пищу по кишечному тракту. Одновременно молекулы АТФ, связывающиеся с P2Y-рецепторами на поверхности клеток, которые выстилают полость кишечника, усиливают секрецию пищеварительных ферментов. Вещества, действующие на эти рецепторы и влияющие на указанные процессы, представляют большой интерес для фармацевтических компаний как возможные кандидаты на роль лекарственных средств, направленных на устранение синдрома раздраженной толстой кишки
и еще более серьезной патологии — болезни Крона.
Тот факт, что АТФ участвует в поддержании нормальной работы множества органов и тканей, предполагает возможность его применения для лечения целого ряда расстройств: болезней почек, костей, мочевого пузыря, кожи, неврологических и психических патологий. И что еще более важно — АТФ, возможно, является одним из естественных защитников организма от онкологических заболеваний. Еще в 1983 г. Элиезер Рапопорт (Eliezer Rapoport), работавший тогда в Медицинской школе Бостонского университета, сообщил о способности АТФ уничтожать раковые клетки. Новость была воспринята с большим скептицизмом, но с тех пор сразу несколько лабораторий независимо друг от друга показали, что АТФ действительно подавляет рост опухолей, в частности предстательной железы, молочных желез, прямой кишки, яичников, пищевода,а также останавливает развитие меланомы. Сигнальная система с участием АТФ, с одной стороны, вызывает апоптоз раковых клеток, а с другой — способствует дифференциации клеток, и все вместе это замедляет рост опухоли.
Для того чтобы новые сведения о функциях АТФ нашли практическое применение — имеется в виду создание лекарственных препаратов, готовых к употреблению, — придется проделать огромную работу. Но уже сейчас многие научно-исследовательские лаборатории и фармацевтические компании активно занимаются поисками веществ, которые избирательно влияли бы на определенные подтипы рецепторов АТФ или блокировали расщепление АТФ после его высвобождения из клеток.
АТФ здесь, АТФ там
Участие АТФ в работе самых разных сигнальных систем ставит перед исследователями по крайней мере одну серьезную проблему: создание лекарственных средств, нацеленных на единственный орган или ткань. Возможно, решить ее поможет разнообразие субъединичных конфигураций АТФ-рецепторов у разных видов клеток и тканей. Балджит Как пытается сейчас сконструировать искусственные АТФ-рецепторы, которые можно было бы встроить в клеточные мембраны in vitro или даже в клетки лабораторных животных. Это позволит выявить последствия минимальных изменений функций рецепторов. Есть и другие подходы к направленному изменению функционирования АТФ как сигнальной молекулы и изучению его последствий на уровне организма.
Одно из недавних достижений последних 20 лет в той области исследований, о которой идет речь, — определение Эриком Гуоксом (Eric Gouaux) из Орегонского университета кристаллической структуры Р2Х-канала у рыбки данио рерио. Теперь мы можем проследить за работой данного рецептора на атомном уровне и понять, как осуществляется АТФ-сигнализация от момента связывания молекулы с рецептором до момента получения сигнала целой физиологической системой. Это поможет также в поиске новых лекарственных средств целевого действия.
Недавно АТФ-рецепторы были обнаружены у растений и таких простейших организмов, как сине-зеленые водоросли, амебы и шистосомы, что открывает новые возможности в борьбе с заболеваниями растений и даже найдет применение в сельском хозяйстве. Наличие систем АТФ-сигнализации у разных форм жизни, далеко отстоящих друг от друга по уровню сложности, наводит на мысль, что коммуникативная функция появилась у АТФ так же давно, как и способность запасать энергию.
Мы с удовлетворением наблюдаем за тем, как изменяется отношение к сигнальной роли АТФ. 50 лет назад сама эта идея считалась несерьезной, а сегодня к АТФ проявляет интерес все биологическое сообщество. Мы уверены, что когда-нибудь возможности АТФ раскроются в полной мере и послужат улучшению качества жизни людей.
Перевод: Н.Н. Шафрановская
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
Molecular Physiology of P2X Receptors and ATP Signalling at Synapses. Baljit S. Khakh in Nature Reviews Neuroscience, Vol. 2, pages 165–174; March 2001.
Pathophysiology and Therapeutic Potential of Purinergic Signaling. Geoffrey Burnstock in Pharmacological Reviews, Vol. 58, No. 1, pages 58–86; March 2006.
Physiology and Pathophysiology of Purinergic Neurotransmission. Geoffrey Burnstock in Physiological Reviews, Vol. 87, No. 2, pages 659–797; April 2007.
Сайт создан в системе
uCoz
 продолжение верхнего рис.
но каждый из них был представлен гораздо большим числом подтипов, чем предполагалось. Такое разнообразие подразумевало, что каждый из подтипов может стать мишенью для «своего» вещества, способного влиять на АТФ-сигналы только в специфических тканях и клетках.
И уже сегодня получены этому подтверждения (табл. на стр. 75).
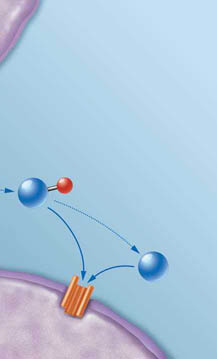
продолжение верхнего рис.
но каждый из них был представлен гораздо большим числом подтипов, чем предполагалось. Такое разнообразие подразумевало, что каждый из подтипов может стать мишенью для «своего» вещества, способного влиять на АТФ-сигналы только в специфических тканях и клетках.
И уже сегодня получены этому подтверждения (табл. на стр. 75). 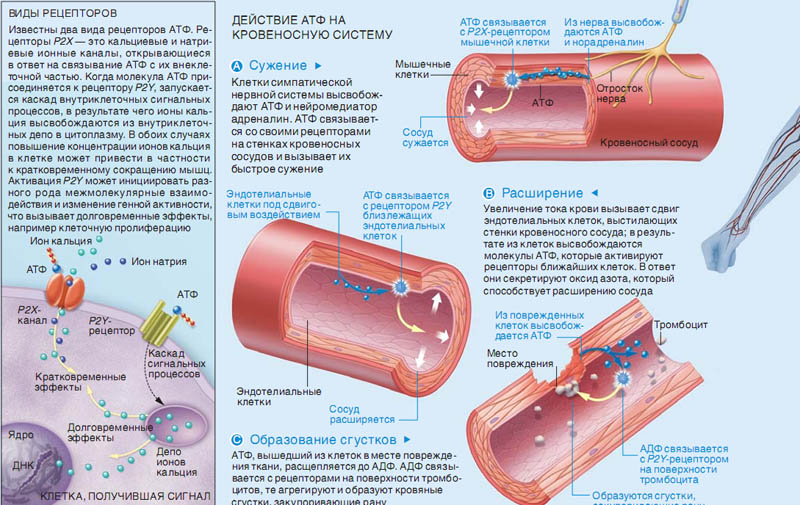
 от одного нейрона другому аденозин может подавлять высвобождение АТФ в синаптическую щель одним из нейронов. Таким образом, взаимное влияние эффектов АТФ, его составляющих и внеклеточных
экто-АТФаз можно рассматривать как основу саморегулирующейся сигнальной сети.
от одного нейрона другому аденозин может подавлять высвобождение АТФ в синаптическую щель одним из нейронов. Таким образом, взаимное влияние эффектов АТФ, его составляющих и внеклеточных
экто-АТФаз можно рассматривать как основу саморегулирующейся сигнальной сети.