Посещений:  ДИАГНОСТИKА
КОРОВЬЕГО БЕШЕНСТВА
ДИАГНОСТИKА
КОРОВЬЕГО БЕШЕНСТВА
|
|
|
Стэнли Прузинер
В Мире Науки, - 2004.- № 10 |
ОБ АВТОРЕ:
Стэнли Прузинер – профессор нейробиологии и биохимии Медицинской школы
Калифорнийского университета в Сан-Франциско, член Национальной академии наук и Американского философского общества. В 1997 г. получил Нобелевскую премию по физиологии и медицине за открытие и исследование прионов.
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА:
Prions. Stanley B. Prusiner. 1997 Nobel Prize lecture. Available from the Nobel Foundation
site at: www.nobel.se/medicine/
Prion Biology and Diseases. Second edition. Edited by Stanley B. Prusiner. Cold Spring Harbor Laboratory Press, 2004.
Advancing Prion Science: Guidance for the National Prion Research Program. Edited by Rick Erdtmann and Laura B. Sivitz. National Academy Press, 2004.
ОТ РЕДАКЦИИ
ТЕСТЫ НА БЕШЕНСТВО
Согласно информации Всемирной
организации здравоохранения, руководящих органов Европейского
союза, Международного эпизоотического бюро, в последние годы
в европейских странах значительно увеличилось количество заболеваний
спонгиоформной энцефалопатией крупного рогатого скота. В период
с 1986 по 2003 г. только в Великобритании был зарегистрирован
183 191 случай, более 1300 – в Ирландии и более 800 – во Франции,
Португалии. Отмечается рост заболеваемости в Бельгии, Германии,
Испании, Швейцарии, а в 2003 г. коровье бешенство было обнаружено
в США. По состоянию на 1 декабря 2003 г., болезнью Крейтцфельдта Якоба (БКЯ), вызываемой прионами, в мире заболело153 человека: 6 – во
Франции, 1 – в Канаде, 1 – в Ирландии, 1 – в Италии, 1 – в США
и 143 – в Великобритании. Многие страны отказываются от импорта
говядины из стран, где отмечены вспышки коровьего бешенства.
Россия закупает за рубежом больше половины потребляемой говядины. Основные поставщики – Австрия, Бельгия, ФРГ, Голландия,
Дания, Испания, Польша, Франция, США и Китай. Сейчас запрещен
ввоз говядины из Великобритании,Португалии, Швейцарии, а ее отгрузка из стран ЕС должна проходить под контролем российского ветврача. Частичные ограничения введены на поставки из Ирландии и Франции.
А ввоз говяжьих субпродуктов из большинства стран ЕС запрещен.
Многие исследователи связывают появление и распространение
прионных заболеваний в Великобритании и в других странах
Европы с использованием мясокостной муки, полученной при переработке больных и павших животных, в том числе овец, пораженных скрепи. Минздрав и Департамент ветеринарии Минсельхоза России издали
ряд методических и правовых актов, запрещающих ввоз мясокостной
и костной муки для использования в качестве кормовых добавок из
неблагополучных по ГЭ и скрепи овец стран. Ввоз животных, кормов, продуктов и сырья животного происхождения в Россию возможен
только с письменного разрешения Департамента ветеринарии. Введен
лабораторный контроль за содержанием животных компонентов в ком-
бикормах, мясной и рыбной муке.
Возбудитель губчатой энцефалопатии – белок, названный прионом.
В принципе он содержится в любом организме и выполняет определенные
функции: регулирует обмен меди, процессы окисления и старения. Но измененный прион, попадающий в организм человека вместе с зараженным
мясом, запускает процесс превращения нормального белка в аномальный.
Как считают ученые, от зараженных коровьим бешенством животных инфекция передается людям и вызывает болезнь Крейтцфельдта–Якоба. Хотя
достоверных методов прижизненной диагностики БКЯ у людей не существует, а иммунитет человека не в состоянии отличить «бешеные» прионы от нормальных.
Сейчас в национальном центре контроля болезней, вызванных прионами, Западного резервного университета США, где осуществляется
вскрытие мозга, проводятся исследования, позволяющие определить,
умер человек в результате заражения от бешеных коров или от оленей
и лосей с хронической атрофией. Возможно, они помогут пролить свет
на источники распространения заболевания.
Чтобы не допустить возникновения болезни на территории России,
в 2004 г. было принято постановление главного государственного санитарного врача РФ от 13.01.2004 г. №1 «Об усилении мер по предуп-
реждению болезни КрейтцфельдтаЯкоба на территории Российской
Федерации».
Прижизненной диагностики заболевания у животных в мире нет, его определяют либо по клиническому течению и поведению, либо посмертным
исследованием мозга. Применяемые методы экспресс-анализа не дают надежных результатов в определении заболевания у большинства забиваемых животных. Наиболее достоверны они в тех случаях, когда в мозге уже накопилось достаточное для выявления болезни количество прионов.
В США большинство животных уже к 24 месяцам набирают вес, при котором они идут на убой, то есть до того, как тесты на бешенство могут дать надежные результаты. В европейских странах обычно обследуют животных от 30 месяцев и старше. Применение современных методов тестирования ко всем идущим на убой животным, 80% которых не достигли 30 месяцев, может привести к необоснованной уверенности в качестве говядины. Оправданна ли экономически и нравственно такая стратегия?
Тестирование одного животного в США обходится в $25–35, что увеличивает стоимость каждого килограмма мяса на несколько центов, а ежегодные расходы – на $1 млрд. Поэтому, как считают эксперты, американцам, как и европейцам, следует проверять животных в возрасте старше 30 месяцев. Министерство сельского хозяйства США предполагает исследовать в этом году по крайней мере 200 тыс. голов крупного рогатого скота, что соответствует числу животных, имеющих заболевания суставов. Возможно, новые исследования, о которых рассказывается в статье «Диагностика коровьего бешенства», позволят обнаруживать при-
оны у молодняка и в тех органах взрослого крупного рогатого скота,
которые раньше считались неинфицированными. А также помогут
ставить точные диагнозы при обследовании людей с подозрениями на БКЯ. Однако только после подтверждения полученных данных
будет иметь смысл тестировать всех животных. В настоящее время более оправданны другие меры.
|
В декабре прошлого года в США был официально зарегистрирован первый случай коровьего бешенства: в штате Вашингтон от губчатой энцефалопатии домашнего скота (ГЭДС – научное название болезни) умерла корова голштинской породы. Эта новость серьезно озаботила ученых, правительство, фермеров, общественность. Однако для тех, кто непосредственно занимается изучением ГЭДС и сходных с ней
патологий, она не стала неожиданностью. Странное поведение прионов
(патогенных факторов, ответственных за эти заболевания) навело ученых на мысль, что контролировать болезнь и сдерживать ее распространение
крайне трудно.
Необычайно долгий инкубационный период коровьего бешенства
(годы, а иногда и десятилетия) заставил исследователей заняться разработкой методов выявления болезни, которые помогали бы предотвращать эпидемии. Уже созданы высокочувствительные тесты, способные обнаруживать прионы в организме животных, не проявляющих никаких симптомов заболевания (до сих пор ГЭДС диагностировали только посмертно).
Достигнуты некоторые успехи и в лечении смертельно опасной для человека болезни Крейтцфельдта–Якоба (БКЯ), также имеющей прионную
природу.
Отчего
возникает прионная болезнь?
Еще в начале 1980-х гг. я предположил, что патоген, вызывающий скрепи у овец (аналог ГЭДС) и болезнь Крейтцфельдта-Якоба у человека, – это белок (я назвал его прионом). Прионная теория была встречена
в штыки, поскольку противоречила общепринятой точке зрения, что
любой патоген, способный к самовоспроизведению, должен содержать
ДНК или РНК. Ничего удивительного в такой реакции не было – это участь
любой слишком смелой идеи. И все же прионная теория оказалась верной.
Прошли годы, и таинственный белок был обнаружен. Сегодня мы знаем, что
различные прионы вызывают не только скрепи и БКЯ, но и другие формы
губчатой энцефалопатии, в том числе коровье бешенство и хроническую изнуряющую болезнь у оленей и лосей. Но еще более удивительным
оказалось то, что прионные белки (PrP) бывают не только «плохими»,
но и «хорошими». Ген, кодирующий нормальный прион (PrPC, С – от англ.
cellular, клеточный), обнаружен в геноме всех исследованных животных.
Он изобилует в нейронах головного мозга и принимает участие в их функционировании. Его аномальный аналог (PrPSc, Sc – от англ. scrapi, скрепи), имеющий другую пространственную конфигурацию, в отличие от PrPC, образует плохорастворимые сгустки, которые не разрушаются ни при тепловой обработке, ни под действием ионизирующей радиации и химических агентов – факторов, уничтожающих обычные патогены (так, кипячение в течение нескольких минут убивает вирусы и бактерии, но не разрушает PrPSc). Более того, аномальный прион изменяет конформацию нормального по своему образу и подобию – превращает его в PrPSc. Обычно клетки распознают белки с неправильной конформацией и разрушают их, но если освобождение от аномальных прионов замедляется, то они накапливаются в клетке и убивают ее. В мозгу больного животного образуются микроскопические вакуоли, и через некоторое время он становится похожим на губку.
Механизмы возникновения прионной болезни бывают разными. Чаще
всего она носит спонтанный характер – такова, например, спорадическая
форма болезни Крейтцфельдта–Якоба, встречающаяся у одного человека на
миллион. Но причиной прионной болезни может стать и мутация в гене,
кодирующем PrP. Во многих семьях, где были случаи заболевания БКЯ, отмечались и другие патологии: болезнь Герстмана–Штресслера–Шайнкера
и фатальная инсомния. На сегодня обнаружено более 30 мутаций в гене PrP, ассоциированных с наследственными формами прионных заболеваний,
каждое из которых встречается с частотой 1 на 10 млн. человек. И наконец, прионная болезнь может возникнуть из-за инфекции, связанной, например, с попаданием в организм аномальных прионов вместе с мясом больного животного.
Распространенность
коровьего бешенства
Опасность прионных болезней стала очевидной после вспышки коровьего бешенства в середине 1980-х гг. в Великобритании. Необычные свойства прионов заставили ученых искать новые способы борьбы с эпидемией. Выяснилось, что прионы попадают в организм коров вместе с добавками к кормам, изготавливаемыми из костей и мяса овец, крупного рогатого
| | |
Прионы существуют в двух разных формах – нормальной (PrPC ) и видоизмененной (PrPSc ). По неустановленной пока причине патогенный прион изменяет конформацию нормального приона по своему образу и подобию. Обычно организм уничтожает видоизмененные прионы прежде, чем они успевают накопиться. Но если процесс уничтожения нарушен, то аномальных прионов становится слишком много и возникает болезн/
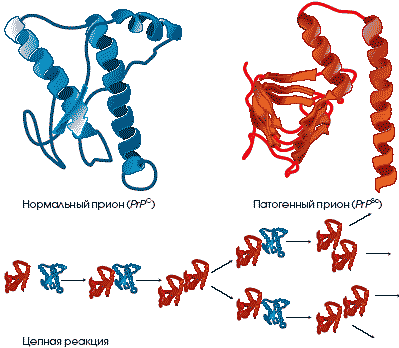
|
|
скота, свиней или кур. Патогенные прионы не разрушались при тепловой
обработке, обычно уничтожающей все болезнетворные агенты, и таким
образом инфицировали животных. В результате ГЭДС стала быстро распространяться в популяции коров, и в 1992 г. в Великобритании было
зарегистрировано 37280 случаев заболевания. Начиная с 1989 г. были введены некоторые ограничения на добавки к кормам, но только в 1996 г. после полного их запрета ситуацию удалось взять под контроль, и в прошлом году в стране заболели лишь 612 животных. Всего в Великобритании от ГЭДС пострадали более 180 тыс. коров, а еще
у 1,9 млн., согласно эпидемиологическим моделям, инфекция просто не
была выявлена.
Однако меры были приняты с большим опозданием. Вопреки заверени-
ям властей, ГЭДС поражает не только животных, но и людей. В марте 1996 г. Роберт Уилл (Robert Will), Джеймс Айронсайд (James Ironside) и Джин Белл (Jeanne Bell) из Национального центра по наблюдению за распространением БКЯ сообщили о смерти 11 молодых людей от вариантной болезни Крейтцфельдта–Якоба (вБКЯ). Обнаруженный в их головном мозге
PrPSc существенно отличался от аномального приона, обычно присутст-
вующего у больных спорадической формой БКЯ.
Многие ученые поначалу сомневались в наличии связи между ГЭДС
и вБКЯ, но в конце концов, под давлением неоспоримых фактов, сомнения
были развеяны. Майкл Скотт (Michael Scott) и Стивен д’Армон (Stephen
DeArmond) из Калифорнийского университета встроили в геном мышей PrP-ген крупного рогатого скота, а затем ввели им прионы, полученные от животных с ГЭДС или от людей, страдающих вариантной формой
БКЯ. Спустя 9 месяцев после инъекции мыши заболели, причем симптомы
были одинаковыми независимо от источника аномальных прионов.
В феврале этого года появились сообщения о 146 случаях заболевания
вариантной формой БКЯ в Англии и 10 случаях в других странах. Сколько
еще людей стали носителями аномальных прионов (возбудителей вБКЯ), не
знает никто. По прогнозам, основанным на эпидемиологических моделях, их не больше 30 человек, но беда в том, что сами модели основываются
на допущениях, которые вполне могут оказаться неверными. Так, одно из них состоит в том, что вБКЯ развивается только у людей с определенным генетическим статусом. Поскольку у прионных болезней очень большой ин-
кубационный период, должно пройти немалое время, пока проявятся все
случаи носительства вБКЯ-прионов и можно будет сравнить генетические
особенности больных.
У больных вБКЯ PrPSc накапливаются не только в тканях головного мозга, но и в лимфоидных тканях, что может быть вызвано их попаданием в кровоток из внешнего источника, например, при переливании крови. Это побудило правительства многих стран ввести более строгие требования к донорам. Так, в Великобритании людям, родившимся после 1996 г., когда вступили в силу жесткие ограничения на добавки к кормам для скота, можно переливать кровь только от доноров из
других стран (считается, что те, кто родились раньше, уже могли получить аномальные прионы). В США же донорами не могут быть люди, проведшие в Великобритании более трех месяцев в период с 1980 по 1996 гг. Принятые меры дали результаты, хотя и привели к тому, что время от
времени в стране возникал дефицит крови. В декабре прошлого года в Великобритании умер один из 15 больных вБКЯ, которым была перелита
кровь от доноров, заболевших позже. При этом гемотрансфузия была проведена пациенту за 7,5 лет до его смерти. Можно было бы предположить, что источником инфекции были пищевые продукты, содержащие аномальные прионы, но этому противоречил возраст умершего: ему было 69 лет, а возраст большинства больных вБКЯ не превышает 29 лет. Все это наводит на мысль, что зараженное прионами
мясо – вовсе не единственный источник инфекции.
Коровье бешенство затронуло не только Великобританию, но и США
и Канаду. В мае 2003 г. канадские власти сообщили о случае заболевания ГЭДС 8,5-летней коровы из провинции Саскачеван, которая была привезена из Великобритании 10 лет назад. Животное было забито в январе 2003 г., а соответствующие тесты были проведены лишь в апреле. А между тем коровью тушу уже переработали в корма для домашних животных и экспортировали их в США. Спустя семь месяцев министерство сельского хозяйства США сообщило о первом случае коровьего бешенства в стране – произошло это в штате Вашингтон. Больная 6,5-летняя дойная корова была привезена в страну
в возрасте четырех лет. Теперь власти США не могут утверждать, что никакого коровьего бешенства в стране нет и населению не о чем беспокоиться.
В Америке, как и в Канаде, многие заинтересованы в том, чтобы проблемы не существовало – ведь это грозит огромными убытками. В первую очередь они связаны с ограничением экспорта: 58 стран уже объявили о закрытии своих рынков для американской говядины до тех пор, пока не будут получены гарантии ее безопасности.
Методы диагностики Самый прямой способ предоставления таких гарантий – проверка на присутствие аномальных прионов туш забитых животных и отбраковка тех из них, которые содержат прионы. До сих пор для тестирования министерство сельского хозяйства США использовало иммуногистохимические методы. Это трудоемкая процедура, занимающая несколько дней и малопригодная для широкого применения.
Нужно было разработать альтернативные способы проверки. В середине
1980-х гг. в нескольких лабораториях были получены новые типы антител,
обеспечивающие более эффективную идентификацию аномальных при-
онов в тканях мозга. Они распознавали любые прионы – как нормальные,
так и патогенные, и чтобы идентифицировать именно PrPSc, нужно было
прежде всего удалить из образца абсолютно все нормальные прионы. Для
этого мы использовали протеиназы – ферменты, разрушающие белки. PrPSc
устойчив к действию протеиназ и после обработки ими образца оставался
| |
|
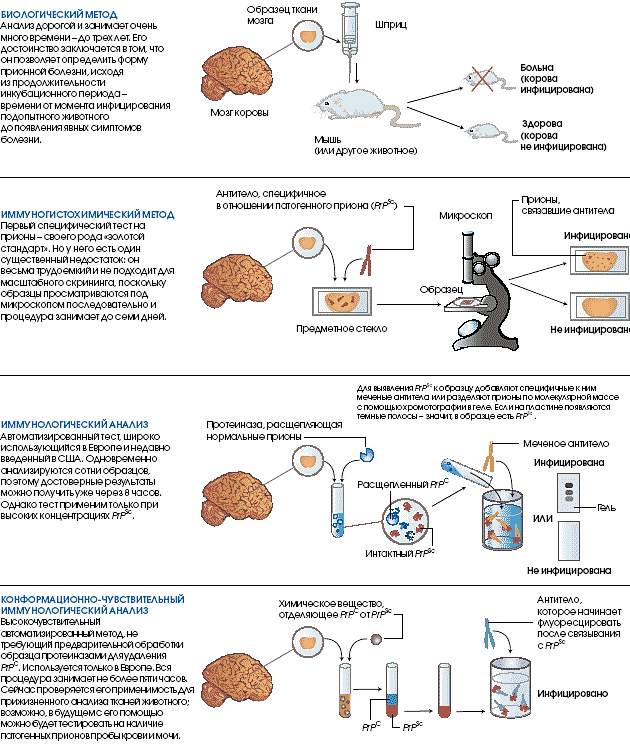
Сегодня для посмертного обнаружения патогенных прионов (PrPSc)
в тканях головного мозга домашнего скота используют четыре мето-
да. К сожалению, у них есть недостатки: трудоемкость, невысокая
чувствительность, обязательное использование для тестирования
препаратов головного мозга. Поэтому ученые работают над созда-
нием таких способов тестирования, которые позволили бы прово-
дить прижизненные экспресс-анализы на основе проб крови или
мочи и выявлять патогенные прионы при минимальной их концентра-
ции. Это необходимо для обнаружения инфекции на самых ранних
стадиях и предотвращения ее распространения.
|
интактным. Затем мы инкубировали образец с антителами и определяли количество присутствующих в нем PrPSc. Используя аналогичный подход, целый ряд компаний разработал собственные варианты антител и набор необходимых для тестирования реактивов. Вся процедура занимает несколько часов и применяется для массового обследования животных в Европе и Японии. (Первый случай коровьего бешенства в Японии был отмечен в 2001 г., а к апрелю этого года число инфицирован-
ных коров достигло 11.) Однако методы быстрого тестирования имеют свои ограничения: их можно применять только когда аномальные прионы присутствуют в головном мозге животного в большом количестве. А поскольку инкубационный период ГЭДС составляет 3–5 лет, у большинства предназначенных на убой коров (как правило, это животные моложе двух лет), даже если они инфицированы, прионы не успевают накопиться до необходимого для проверки уровня. Следовательно, упомянутые тесты пригодны для скрининга коров только старше определенного возраста, при этом в первую очередь тестированию подлежат вялые, апатичные животные, а затем и те, которые выглядят вполне здоровыми.
До января нынешнего года, когда в США были введены новые правила
контроля, из 200 тыс. туш ослабленных коров, ежегодно отправляемых на мясоперерабатывающие комбинаты, исследовали на наличие прионов лишь
небольшую часть. Теперь, согласно новым требованиям министерства сельского хозяйства, проверке подлежат все забиваемые животные. (Вопрос о том, может ли коровье молоко служить источником прионов, остается открытым.) Но поскольку даже новые методы тестирования не удовлетворяют всем необходимым требованиям, первоочередной задачей становится разработка новых подходов к идентификации аномальных прионов.
СПОНТАННАЯ ПРИОННАЯ БОЛЕЗНЬ
Заболевания, имеющие прионную природу, похожи на вирусную инфекцию, поэтому прионы нередко сравнивают с вирусами. Однако такая аналогия не совсем корректна. В качестве примера можно привести случаи появления коровьего бешенства в Канаде и США. Принято считать, что заболевание, впервые зарегистрированное в Великобритании, распространилось по всему земному шару через зараженное мясо забитых коров, но это справедливо лишь отчасти. Дело в том, что прионная болезнь иногда возникает спонтанно, и это в корне отличает ее от вирусных инфекций, очаг которых можно изолировать. Аномальный же прион может появиться в самом организме, а не попасть в него извне.
Спонтанное прионное заболевание стало спусковым механизмом для
эпидемии куру, разразившейся в прошлом веке в одном из племен Новой
Гвинеи. У одного из членов племени возникла спонтанная форма болезни
Крейтцфельдта–Якоба, и когда он умер, его мозг был съеден ближайшим
другом, как того требовал ритуал. Поскольку в племени был распространен каннибализм, возникла эпидемия.
Для того чтобы остановить распространение коровьего бешенства,
необходимо отказаться от практики добавления в корм животных продук-
тов переработки туш забитых коров. Но это не может искоренить болезнь,
поскольку патогенные прионы все равно будут время от времени появляться спонтанно. Некоторые ученые считают, что те два случая заболевания коровьим бешенством, о которых стало известно в конце прошлого года, были проявлением спонтанной формы прионной болезни и что такие инциденты случались и ранее.
Впрочем, иные полагают, что заболевшие коровы из Северной Америки
получили прионы с кормом. Тем самым поддерживается точка зрения, что
прионы – это белковый аналог вирусов, т.е. они являются инфекционными
агентами (хотя известно, что прионные болезни могут носить наследственный характер или возникать спонтанно). А раз так, то коровье бешенство можно искоренить, вводя строгие карантинные меры. Не обращая внимания на новейшие данные, касающиеся биологии прионов, можно помешать созданию эффективной программы по защите населения США от смертоносных агентов. Нужно не ограничиваться введением карантина и строгих мер контроля, а проводить масштабное тестирование на наличие прионов, пока не разразилась эпидемия. |
Один из таких способов мог бы состоять в амплификации аномальных
прионов, присутствующих в исследуемом образце, до концентрации, поддающейся измерению. В случае успеха можно было бы использовать для
анализа пробы крови, а не головной мозг животного (нынешние методы
недостаточно чувствительны, чтобы обнаружить следовые количества PrPSc
в крови). Клаудио Сото (Claudio Soto) из Serono Pharmaceutical в Италии уже попытался реализовать эту идею. Он смешал образцы тканей мозга двух хомяков (здорового и больного скрепи) и обработал смесь ультразвуком, с тем чтобы дезинтегрировать сгустки PrPSc. Высвободившиеся молекулы аномального приона тут же трансформировали нормальные молекулы, и в результате доля нечувствительных
к протеиназам PrPSc в образце увеличивалась в 10 раз. В основе альтернативного подхода лежит использование особенностей конформации аномальных прионов, а не их амплификация. Так, в одном из
тестов мы с моими коллегами применили антитела, способные связываться
либо с PrPC, либо с PrPSc, но не с обоими прионами. Мишенью антитела
служила часть прионовой молекулы, доступная при одной ее конформации и недоступная при другой. Такой способ тестирования не требует этапа
протеиназной обработки, что очень важно, поскольку, как оказалось, одна из форм PrPSc чувствительна к протеиназам, и, обрабатывая ими образец для разрушения PrPС, мы разрушали и аномальные прионы и тем самым недооценивали их количество.
| |
|
РАЗНООБРАЗИЕ ПРИОНОВ
Одна из особенностей прионов, делающая их похожими на вирусы, – разно-
образие форм. Прионы, как и вирусы, могут принадлежать к разным «штам-
мам», слегка отличающимся друг от друга. Штамм в данном случае – это
PrPSc с определенной конформацией. Как она связана с биологическими
свойствами приона – никому не известно, хотя вызываемые разными прионными штаммами заболевания различаются. Что касается человека, то такие патологии, как болезнь Крейтцфельдта–Якоба, куру, фатальная инсомния и болезнь Гертсмана–Штресслера–Шайнкера, ассоциированы с патогенными прионами разных штаммов, а скрепи у овец вызывают прионы 20 разновидностей. Возможно, и ГЭДС – это не одно, а целая группа сходных, но все же не идентичных заболеваний. Так, у 23-месячной коровы из Японии и одной коровы из Словакии PrPSc был сконцентрирован в среднем мозге, в то время как в большинстве известных случаев он накапливался в стволе головного мозга.
Необходимость идентификации прионовых штаммов стала очевидной
после того, как были проведены эксперименты на овцах, которым вводили
ГЭДС-прионы. Овцы одной из пород, имеющие генотип ARR/ARR (буквы
обозначают аминокислоты в молекуле приона), устойчивые к скрепи, заболели после введения им ГЭДС-прионов. Тот факт, что животные могут быть невосприимчивы к одним прионам и чувствительны к другим, имеет большое значение для фермеров, занимающихся их разведением.
В некоторых европейских странах созданы программы по искоренению
скрепи, в основе которых лежит скрещивание между собой овец с генотипом ARR/ARR. Однако создание таких генетически однородных популяций только повышает риск появления овец, несущих ГЭДС-прионы. А это, в свою очередь, создает серьезную угрозу людям, употребляющим в пищу баранину: в отличие от прионов, вызывающих скрепи, ГЭДС-прионы опасны для человека. Прежде чем реализовывать упомянутые программы, следует провести эксперименты на мышах, с тем чтобы сравнить патогенность ГЭДС-прионов, полученных от овец и от коров. |
Наш тест, который мы назвали конформационно-чувствительным имму-
нологическим анализом (conformationdependent immunoassay, CDI), был
разрешен к применению в Европе в 2003 г., и не исключено, что его чувствительности будет достаточно для определения PrPSc в пробах крови. Уже доказана возможность применения нового теста для проверки молодых коров. Так, из Японии осенью 2003 г. поступило сообщение о возможном заболевании ГЭДС двух коров в возрасте 21 и 23 месяцев, не проявляющих никаких признаков неврологических нарушений. Подтвердить диагноз у второй из них удалось только с помощью CDI-теста – в стволе мозга у нее были обнаружены скопления аномальных прионов. Обычные тесты на PrPSc дали неоднозначные результаты.
В Европе проверке на наличие аномальных прионов подлежит крупный
рогатый скот в возрасте более 30 месяцев, если он предназначается на убой (в Германии порог ниже – 24 месяца), поэтому случай, аналогичный произошедшему в Японии, там был бы невозможен. Вначале правительство
Японии намеревалось ввести у себя в стране правила тестирования, принятые Европейским союзом, но адвокаты потребителей настояли на том,
чтобы проверку проходило каждое забитое животное.
Многоликие и вездесущие
Работая над созданием теста, мы выявили один интересный факт. Как уже
упоминалось, популяция прионов весьма неоднородна – это семейство
белков с разной устойчивостью к протеиназам. Более того, оказалось, что чувствительные к протеиназам формы PrPSc появляются в организме гораздо раньше, чем устойчивые. Может быть, первые из упомянутых форм – предшественники вторых? Ответить на вопрос мы пока не можем. Так или
иначе, только тесты, способные обнаруживать чувствительные к протеиназам прионы, позволят диагностировать болезнь задолго до появления симптомов и тем самым предотвратить попадание на рынок зараженных мясных продуктов и вовремя начать лечение инфицированных больных. К счастью, CDI-тест дает возможность обнаруживать чувствительные к протеиназам формы PrPSc в крови грызунов и людей, страдающих БКЯ, даже при очень низкой их концентрации.
Охота за прионами, попавшими в кровь, принесла еще один сюрприз.
Вместе с Патриком Боском (Patrick Bosque) из Колорадского центра здравоохранения мы обнаружили прионы в мышцах задних конечностей мыши
в концентрации, в 100 тыс. раз большей, чем в крови (прионы присутствовали и в мышцах других групп, но в гораздо меньшем количестве). Майкл Бикс (Michael Beekes) из Института Роберта Коха в Берлине обнаружил высокую концентрацию PrPSc почти во всех мышцах хомяков, в корм которым добавлялись эти белки. Ученые из Калифорнийского университета в Сан-Франциско Сафар и д’Армон
нашли PrPSc в мышечных тканях некоторых больных, страдающих БКЯ.
Новые методы терапии
Новые методы диагностики, несомненно, помогут обезопасить население от заражения прионами через мясные продукты или переливаемую кровь, но это вряд ли принесет утешение тем, кто уже болен смертельным недугом.
Поэтому следующая цель ученых – поиск способов блокирования процесса трансформации нормальных прионов в патогенные или повышение эффективности их разрушения в клетке. На сегодня идентифицировано более 20 соединений, либо подавляющих образование аномальных прионов, либо ускоряющих их устранение в культуре клеток. Некоторые из соединений продлевают жизнь мышам и хомякам, когда они вводятся им вскоре после инокуляции прионов, но ни одно не влияет на ход патологического процесса, если лечение начато с опозданием. К тому же многие соединения необходимо вводить в высоких дозах, что небезопасно для организма.
Лекарственные препараты должны преодолевать гематоэнцефалический
барьер и проникать из крови в головной мозг. Карстин Курт (Carsten
Korth) из Калифорнийского университета Сан-Франциско, Каэдзуми Дахура
(Katsumi Doh-ura) из Университета Киушу в Японии и Байрон Коги (Byron
Caughey) из Национального института по исследованию аллергии и инфек-
ционных болезней независимо друг от друга показали, что некоторые из уже известных препаратов, действующих на головной мозг, такие как торазин (его применяют для лечения шизофрении), подавляют трансформацию прионов в культуре клеток. Еще более эффективен противомалярийный агент хинакрин, близкий по структуре к торазину.
Хинакрин оказывает слабый положительный эффект в отношении жи-
вотных. Ученые вводили его мышам начиная с 60-х суток после инъекции
в головной мозг аномальных прионов и обнаружили, что инкубационный период у леченых мышей увеличивался на 20%. Мои коллеги из Калифорнийского университета Сан-Франциско Барнаби Мэй (Barnaby May) и Фрэд Коэн (Fred E.Cohen) попытались повысить эффективность действия хинакрина. Для этого они соединили вместе две его молекулы и показали, что такой димер в 10 раз более активен, чем обычный
хинакрин.
Другой подход к лечению состоит в использовании антител, подавляющих образование PrPSc в культуре клеток. Обнаружено, что при введении антител мышам, которым предварительно в кишечник (а не в головной мозг) были инъецированы прионы, наблюдалось увеличение инкубационного периода. Что касается человека, то антиприонная терапия пока была применена лишь в нескольких случаях: это больные БКЯ, а также спонтанной и генетически обусловленной формами, которые получали хинакрин перорально. Конечно, вылечить их не удалось, но жизнь их была на какое-то время продлена.
Врачи попытались использовать для лечения больных вариантной формой БКЯ пентозанполисульфат – препарат, применяющийся при заболеваниях мочевого пузыря. Молекула этого вещества несет сильный электрический заряд и не может преодолеть гематоэнцефалический барьер, поэтому лекарство вводят непосредственно в один из
желудочков головного мозга. У одного молодого человека, больного вБКЯ, отмечалось некоторое замедление патологического процесса, но вряд ли пентозанполисульфат распространится по всему головному мозгу (по крайней мере, с другими заряженными молекулами этого не происходит), а потому эффект будет незначительным.
Прежде чем делать выводы об эффективности хинакрина и других
противоприонных препаратов, необходимо провести тщательно контролируемые клинические испытания. Трудности могут возникнуть уже на первом этапе, поскольку никто не знает, в каком режиме следует проводить терапию. Так, многие противораковые лекарства вводят периодически, чтобы снизить их токсическое действие.
Дорога к успеху будет долгой и трудной, но наметившийся прогресс дает надежду, что мы пойдем по ней гораздо быстрее, чем пять лет назад. Мы полагаем, что создание эффективных методов борьбы с прионными болезнями послужит предпосылкой к успешному лечению гораздо чаще встречающихся нейродегенеративных расстройств, как болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз.
Сайт создан в системе
uCoz