Notch и его лиганды (Delta, Jagged/Serrate, Lag-2) играют важную роль в развитии нервной системы. Взаимодействие Notch с лигандом дает растриктивный сигнал, который ингибирует генерацию нейробластов из эктодермальных предшественников. Notch сигналы регулируют ранние этапы нейрогенеза, генерацию первичных неронов. Они ограничивают количество клеток, готовых принять нейральную судьбу путем репрессии экспрессии bHLH транскрипционных факторов, таких как neurogenin (Ngn1) и NeuroD.
Помимо этого Notch сигналы участвуют в созревании молодых нейрнов. Notch и Delta необходимы для выживания и нахождения аксонами межсегментных нервов. Кроме того Kuzbanian, протеаза, необходимая для созревания Notch и/или Delta белков, обязательна для аксонального наведения и роста. Расщепление Delta с помощью этой протеазы дает растворимые фрагменты, которые обусловливают втягивание нейритов в кортикальные нейроны. Кроме того Notch и онкогенный продукт Abl способны экспрессироваться в аксонах и ростовых конусах и взаимодействуют синергично для нахождения пути и роста аксона.
Автономная и неавтономная регуляция развития нейритов у млекопитающих с помощью Notch1
Изофофрма Notch1 экспрессируется в нейральных предшественниках и в только что возникших постмитотических нейронах. Экспрессия Notch1 сохраняется в большинстве нейронов млекопитающих в течение всей жизни. Взаимоотношения между Notch и presenilin указывают на то, что Notch сигналы могут быть важны в этиологии нейродегенеративного заболевания, болезни Алцгеймера.
N2a клетки нейробластомы, экспрессирующие активированную форму Notch, Notch1IC, дают короткие нейриты, тогда как N2a клетки, экспрессирующие доминантно-негативную Notch1 или доминантно-негативную Delta1 конструкцию, дают длинные нейриты с большим числом первичных нейритов. Было установлено, что N2a клетки, ко-культивируемые с Delta1-экспрессирующими клетками перепела, продуцируют мало или короткие неритные отростки. С другой стороны, высокий уровень Deltа1, экспрессируемый самими N2a клетками, стимулирует рост нейритов и увеличивает количество первичных нейритов и индуцирует экспрессию Jagged1 и Notch1.
Полученные результаты указывают на то, что Notch1 и лиганд =- возможно Jagged1 - взаимодействуют в клетках нейробластомы и контролируют элонгацию нейритов (рис.1а).
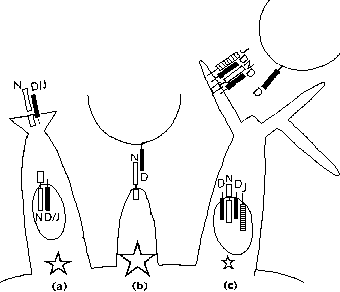

Предполагаемая модель cis и trans эффектов Delta 1 на нейриты. (а) Взаимодействие эндогенных Notch с лигандом регулирует вырост нейритического отростка без влияния со стороны лиганда соседней клетки. N, Notch1; D, Delta1; J, Jagged1. (b) Лиганды, экспрессируемые клеткми вдоль пути миграции репрессируют вырост нейрита, экспрессирующего Notch1. (с) Высокие уровни Delta1 ингибируют рецепцию лингандов вдоль пути миграции, индуцируя Jagged1 и Notch1 и усиливая вырост нейритов. Относительные размеры звездочек указывают на предполагаемые количества передаваемых сигналов Notch.
Как Jagged1 регулирует рост неритов и Notch сигналы неясно, но предполагается, что Delta1 и Jagged1 функционируют сходным образом. Следовательно, возможно, что происходит лиганд-независимая активация Notch и ингибируется она с помощью доминантно-негативных изоформ Notch.
По данным на дрозофиле предложена модель, согласно которой Delta присутствует вдоль путей миграци аксона и активирует Notch молекулы, экспрессирующиеся в растущем аксоне. Delta1 или Jagged1, как было показано выше, действуя в транс-положении (из соседней клетки), напоминают действие контакт-опосредующих или растворимых хеморепульсивных факторов, которые активируя Notch молекулы ингибируют вырост нейритов.
Однако Delta1 белок, экспрессируемый на высоком уровне в самой нейробластомной клетке усиливает вырост нейритов. Очевидно Delta1 молекулы, экспрессируемые шт сшы имеют доминантно-негативный эффект на Notch1 сигналы. Механизм ингибирования неясен, предполагается, что димеризация гомотипического лиганда обусловливает его секвестрацию.
Как Notch сигналы регулируют рост нейриттов? В большинстве случаев эффекты Notch опосредуются через CSL белки (CBF, SuH, Lag1), которые регулируют экспрессию генов вместе с внутриклеточным доменом Notch. Очевидно, что сигналы Notcn поступают в ядро.
Notch взаимодействует синергично с Abl тирозин киназой, регулируя нахождение пути специфическим аксоном. Sanpodo является другим возможным медиатором Notch регуляции развития нейритов через его взаимодействие с цитоскелетом. Итак, можно предположить, что Notch осуществляет свое влияние на рост нейритов через локальные модуляторы цитоскелета, такие как Sanpodo или Abl скорее, чем через ядерные эффекты. В последнем случае необходимо чтобы активированные фрагменты перемещались на большие расстояния от ростового конуса в ядро. Но могут интегрированно действовать оба механизма.