Хламидии, внутриклеточные паразиты, вызывают серьезные офтальмологические патологии, пневмонию, бесплодие и даже влияют на возникновение сердечно-сосудистых заболеваний. Исследователи надеются, что вскоре они смогут сдерживать распространение этих микроорганизмов.
Возбудителями болезни служат крошечные микроорганизмы
рода Chlamydia. При этом штамм C. trachomatis вызывает конъюнктивит и трахому (а также инфекции, передающиеся половым путем), штамм C. pneumoniae – фарингит, бронхит и пневмонию. Установлена даже связь между инфекцией C. pneumoniae и развитием атеросклероза (сужением кровеносных
сосудов, приводящим к инфарктам и инсультам) (см. табл. на стр. 57).
Для борьбы с хламидиями можно использовать антибиотики. К сожалению, хламидиозы (например, урогенитальные инфекции) часто протекают бессимптомно, и лечение начинают слишком поздно. В развивающихся же странах, население которых страдает от трахомы, часто недостает самых обычных средств личной гигиены и медикаментов. В результате многие из 600 млн. человек, инфицированных одним или несколькими штаммами Chlamydia,
не получают медицинской помощи до тех пор, пока процесс не зайдет слишком далеко и не станет необратимым. Вряд ли врачи когда-либо смогут
выявить всех носителей хламидий, передающихся половым путем,
а уровень гигиены в странах третьего мира повысится настолько,
что там удастся остановить распространение трахомы. Поэтому
остается надеяться только на создание эффективной вакцины против
хламидиозов. Чтобы найти агенты,способные убить инфекцию в зародыше, необходимо в деталях разобраться в том, как хламидии вызывают инфекцию и функционируют на молекулярном уровне. Однако в разных ситуациях хламидии используют разные стратегии, позволяющие им ускользнуть от иммун-
ной системы организма, а работать с ними in vitro крайне трудно.
Бессимптомная болезнь
Создание вакцины против хламидиозов – чрезвычайно сложная задача.
Дело в том, что этот патоген действует на организм не так, как другие микроорганизмы. Бактерии, вызывающие, например, столбняк или
холеру, насыщают ткани токсинами, которые повреждают или полностью разрушают беззащитные клетки. В отличие от них хламидии не
оказывают на ткани прямого разрушающего воздействия. Проникнув в организм, они вызывают бурный иммунный ответ – воспалительную реакцию, которая продолжается до тех пор, пока остается хотя бы один микроб. По иронии судьбы, такой способ защиты от инфекции в конце концов приводит к повреж-
дению тканей. Обычно вакцинация обеспечивает невосприимчивость
к заражению, нацеливая иммунную систему на строго определенного
агента, но воспалительный компонент иммунного ответа действует не
адресно и в данном случае приносит больше вреда, чем пользы.
Воспаление начинается с того, что особые клетки иммунной системы
секретируют цитокины – небольшие сигнальные белковые молекулы, которые привлекают к очагу инфекции другие клетки с защитными функциями. Вместе с цитокинами они пытаются изолировать очаг и остановить распространение патогена.
Параллельно цитокины запускают процесс заживления тканей, что
приводит к образованию рубцов. Воспаление тканей мочеполовой
системы долго остается незамеченным. Из 3,5 млн. американцев,
инфицированных хламидиями, которые передаются половым путем,
у 85–90% вообще не отмечается никаких симптомов. Мужчины иногда
испытывают дискомфорт при мочеиспускании, а женщины вообще могут ничего не ощущать до тех пор, пока инфекция не распространится
на фаллопиевы трубы. И только когда приходит время подумать о том,
чтобы завести ребенка, женщина понимает, что с ней произошло
несчастье. Постоянное воспаление фаллопиевых труб и образование в них рубцов могут приводить к хроническим болям в области
малого таза и увеличивать риск внематочной беременности – основной
причины смерти женщин в США в первый триместр беременности.
Воспаление век при хламидиозе более заметно. В развивающихся
странах с жарким климатом от этой инфекции страдают 150 млн. человек. В отсутствие лечения и при низком уровне гигиены мухи и комары
мгновенно разносят инфекцию по всей популяции. Нелеченая трахома
постепенно приводит к деформации края век, их завороту или вывороту, неправильному росту ресниц, травмирующих глазное яблоко,
к воспалению и помутнению роговицы, а в конце концов – к потере
зрения.
Учитывая, что наибольший ущерб организму при хламидиозах при
носит воспалительный процесс, при создании вакцины необходимо
найти такой способ контроля поведения бактерии, при котором воспалительная реакция использовалась бы организмом только как способ привлечения других элементов иммунной системы.
Исследователи сосредотачивают все усилия на поиске факторов, которые либо инициируют секрецию цитокинов, либо подавляют воспалительную реакцию, как только инфекция прекратилась. За последние несколько лет ученые обнаружили небольшие молекулы, которые в норме стимулируют или подавляют эти процессы в организме. Теперь нужно найти вещества, способные
регулировать активность упомянутых молекул. Эти вещества можно
было бы вводить в организм с целью искусственного прерывания воспалительного процесса после того, как проведено лечение антибиотиками.
Тупик
Создание эффективной вакцины против хламидиозов затрудняется не только тем, что вакцинация индуцирует непреходящую воспалительную реакцию, но и тем, что приобретенный иммунитет действует только в течение шести
месяцев. Таким образом, болезнь, казалось бы, оставившая человека
навсегда, может вспыхнуть снова через несколько месяцев или спустя годы. Если уж сама природа не создала против хламидиозов механизма долговременной защиты, то вакцина, лишь копирующая этот механизм, в этом не преуспеет.
Организм помнит о встрече с инфекционным агентом благодаря
тому, что после выздоровления в нем остаются так называемые В-лимфо-
циты памяти. Они патрулируют по всем тканям, готовые к синтезу
антител, которые тут же свяжутся с антигенами болезнетворного
агента, если он повторно попадет в организм. Это послужит сигна-
лом к уничтожению патогена еще до того, как он проникнет в здоровые
клетки. Иммунная система отлично справляется со многими патогенами,
чей жизненный цикл протекает вне клетки-хозяина. Антитела могут атаковать
ХЛАМИДИИ ПЕРЕДАЮТСЯ НЕ ТОЛЬКО ПОЛОВЫМ ПУТЕМ
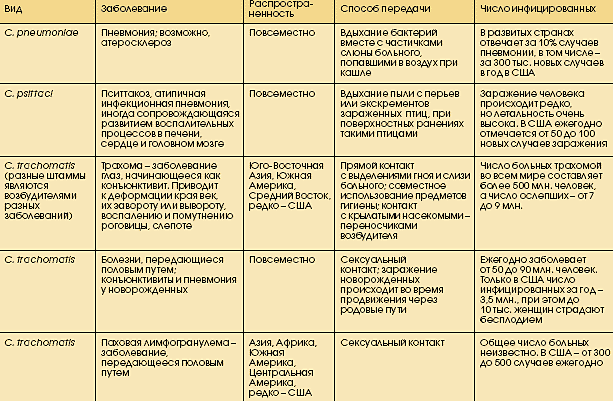
микроорганизм еще и до того, как он проникнет в клетку, или в тот
момент, когда его копия выйдет из клетки, где она образовалась, и отправится на поиски нового хозяина. Но с хламидиями, которые живут
и размножаются внутри клетки, куда не могут проникнуть антитела,
В-лимфоциты не справляются.
Чтобы не дать хламидии спокойно дремать внутри клетки-хозяина, а затем, проснувшись, начать размножаться, нужна вакцина, способная не только вызывать образование антител (гуморальный ответ), но и индуцировать мощный клеточный ответ. Такой компонент иммунной системы, участвующий в уничтожении вирусов (они тоже живут и размножаются внутри клетки-хозяина), включает Т-клетки – киллеры и хелперы, а также клетки-«мусорщики» – макрофаги. К сожалению, даже это трио не способно полностью устранить хламидий. Очень часто инфицированные ими клетки выживают и продолжают
служить источником инфекции.
Создание вакцины, способной превзойти организм в индукции
клеточного ответа, – трудная задача. Большинство существующих вакцин
направлено на запуск синтеза специфических антител, а надежная активация клеточного ответа, распространяющегося на широкий спектр патогенных микроорганизмов, до сих пор остается для ученых недостижимой мечтой. У хламидий есть свои способы защиты от упомянутого компонента иммунной системы.
Невидимый налетчик
Хламидии, как и некоторые другие патогены, оккупируют эпителиальные
клетки: в данном случае слизистую органов мочеполовой системы, век
и легких. Они проникают туда в составе вакуолей, отпочковывающихся
от клеточной мембраны. Обычно здоровые клетки пытаются уничтожить
патогены, обеспечив слияние попавших в клетку вакуолей с лизосомами,
клеточными органеллами, которые содержат ферменты, расщепляющие
белки, липиды и ДНК чужака. Далее клетки размещают продукты расщепления на так называемом главном комплексе гистосовместимости (МНС, от англ. major histocompatibility complex), группе белков, расположенных на клеточной поверхности. Т-клетки, постоянно циркулирующие по всему телу, замечают ком-
плекс МНС и тоже связываются с ним. Получив еще один сигнал от антиген-представляющей клетки, они приходят к окончательному выводу,
что клетка инфицирована, и организовывают на нее атаку.
Но хламидиям в составе вакуолей удается избежать действия лизосом,
и бактерии, будучи физически отделены от остальной части клетки,
беспрепятственно размножаются. Т-клетки не могут узнать об их присутствии, потому что на клеточной поверхности не выставлено никаких опознавательных знаков. Возможно, детально разобравшись в том, как именно растущие бактерии избегают встречи с лизосомами, удастся
найти новые способы сдерживания или искоренения инфекции.
Поможет в этом и секвенирование генома Chlamydia.
Недавно Ру Чинг Шиа (Ru-ching Hsia) и один из авторов этой статьи
(П.Баволи) провели сравнительный анализ геномов Chlamydia и Salmonella
pyphimurium – бактерии, вызывающей пищевое отравление. Сходство
между некоторыми их генами навело на мысль, что у хламидии, как
и у сальмонеллы, есть все необходимое для образования универсальной
структуры, напоминающей иглу, которая известна под названием системы секреции типа III. Эта структура, пронизывающая мембрану вакуоли,
служит каналом, который соединяет бактерию и цитоплазму клетки-хозяина. По нему бактерия инъецирует в цитоплазму особые белки, которые покрывают вакуоль с хламидиями и защищают ее от действия лизосом.
Левая часть верхнего рисунка
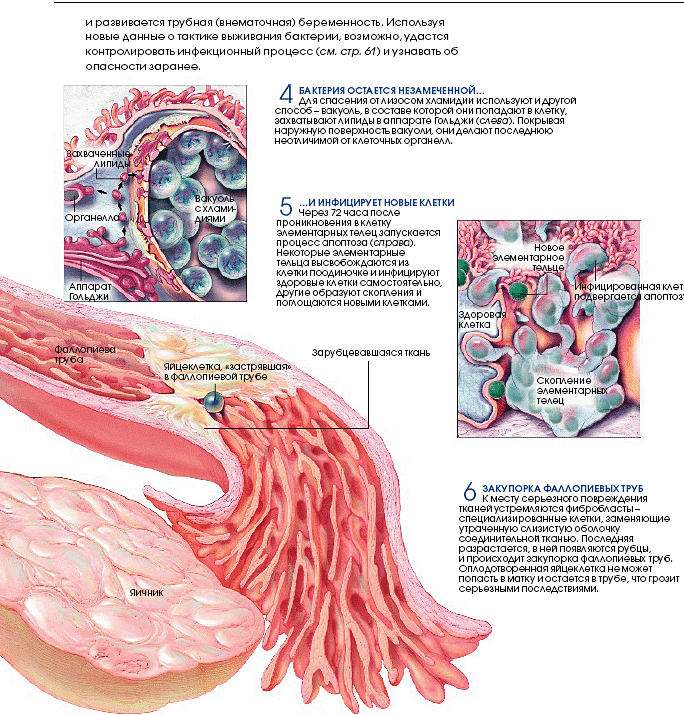
Кроме того, опыты с использованием флуоресцирующих липидов показали, что вакуоль с хламидиями захватывает липидные молекулы некоторых клеточных компартментов (в частности, аппарата Гольджи) и размещает их на своей поверхности. В результате вакуоль становится для клетки-хозяина неотличимой от собственных органелл и невидимой для лизосом.
Когда ученые идентифицируют белки, которыми вакуоль маскирует
мембрану, они смогут повлиять на их активность с тем, чтобы ускорить слияние вакуоли с лизосомой и вызвать иммунный ответ немедленно после
проникновения хламидии в клетку. Также можно попытаться воздействовать на механизм захвата бактерией липидов хозяйской клетки.
Изощренные убийцы
Последние данные о роли Т-клеток вселяют некоторый оптимизм.
Т-киллеры уничтожают инфицированные клетки, побуждая их перейти к апоптозу (запрограммированной гибели). Для саморазрушения (деградации белков и ДНК)
клетки используют собственные ферменты. Известно также, что клетки иммунной системы (в том числе Т-клетки и макрофаги) стимулируют выработку цитокинов, которые помогают нейтрализовать бактерии и вызвать воспалитель-
ную реакцию, останавливающую их распространение. Одним из таких цитокинов двойного назначения служит фактор . некроза опухолей
(TNF-α, от англ. tumor necrosis factorα).
Однако, как показали опыты in vitro, некоторые инфицированные клетки избегают действия TNF-. и других цитокинов, направляющих их на путь апоптоза, и тогда возникает хроническая инфекция. При этом цитокины продолжают поддерживать воспалительный процесс, стараясь хотя бы ограничить
распространение инфекции.
Но даже инфицированные клетки, избежавшие апоптоза, не живут
вечно. Хламидии, по-видимому, выработали собственный способ убийства клеток-хозяев – во имя продолжения рода. (Прежде чем бактерия сможет инфицировать другие клетки, хозяйская клетка должна быть
разрушена.) По данным, полученным Жан-Люком Перфеттини (Jean-
Luc Perfettini) из Пастеровского института в Париже, хламидии могут
|
ХЛАМИДИИ И СЕРДЕЧНО-СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ
Фарингиты, бронхиты, пневмония – это далеко не
все, что угрожает людям, вдохнувшим вместе
с воздухом частички Chlamydia. Как показали
недавние исследования, C. pneumoniae играет роль
в возникновении таких серьезных заболеваний, как
инфаркты и инсульты. Впрочем, у этой стороны есть
и положительная сторона: назначая антибиотики,
врачи могут лечить одновременно инфекционные
и сердечно-сосудистые заболевания.
Атеросклероз (сужение коронарных артерий,
приводящее в большинстве случаев к инфарктам
и инсультам) служит причиной 50% смертей в развитых
странах. Ученые, занимающиеся патогенезом
сердечно-сосудистых заболеваний, заподозрили
в причастности к ним разного рода инфекций сразу
после того, как стало ясно, что воспалительная
реакция, возникающая в ответ на проникновение
в организм инфекционного агента, приводит
к разрастанию бляшек на стенках сосудов.
В 1983 г., после идентификации C. pneumoniae
как отдельного вида хламидий, она стала
рассматриваться как один из кандидатов на роль
провокатора сердечно-сосудистых заболеваний:
антитела к ней обнаруживались у 60% взрослого
населения земного шара. Предположения
подтвердились, когда в 1988 г. врач из Финляндии
сообщил о наличии позитивной корреляции между
присутствием в организме антител к хламидиям
и вероятностью развития сердечно-сосудистых
заболеваний. А через пять лет в закупоренных
артериях больных атеросклерозом были обнаружены
сами бактерии. С тех пор такие организации,
как национальные институты здравоохранения
и Американская ассоциация по сердечным
заболеваниям, выделили миллионы долларов на
исследование роли C. pneumoniae в развитии
атеросклероза.
Опыты на животных, проведенные в последние пять
лет, показали, что хламидии могут перемещаться
из легких мышей в другие части тела в составе
лейкоцитов – клеток, ответственных за возникновение
воспалительной реакции как части иммунного ответа.
Кроме того, обнаружилось, что у мышей и кроликов
в присутствии в организме C. pneumoniae ускоряется
развитие атеросклероза, а прием антибиотиков
замедляет этот процесс.
Полученные предварительные результаты
послужили основанием к проведению ограниченных
клинических испытаний. В трех из пяти подобных работ
было показано, что прием антибиотиков в течение
одного–трех месяцев замедляет прогрессирование
атеросклероза. Но достаточно ли эффективны такие
меры для предотвращения серьезных сердечно-
сосудистых патологий, пока неясно. В 2004 г. неудачей
закончились два испытания (в каждом из них
принимали участие 4 тыс. добровольцев), в которых
пациенты получали антибиотики от одного года до
двух лет.
Доказать роль C. pneumoniae в развитии
атеросклероза у человека очень трудно хотя бы
потому, что это заболевание носит многофакторный
характер.
|
Одни только просветительские меры (информирование населения о безопасном сексе и правилах личной
гигиены) не остановят распространение хламидиозов. Поэтому ученые по-прежнему занимаются
созданием вакцин и поисками других превентивных мер. Здесь перечислены некоторые возможные способы
уничтожения хламидий и уменьшения ущерба, который они наносят организму вследствие неадекватного
иммунного ответа.
УНИЧТОЖЕНИЕ БАКТЕРИЙ У «ВХОДНЫХ ВОРОТ»
Создание противомикробного препарата местного
применения (геля, крема или пенящейся массы) для
вагинального или ректального введения. Сходные средства,
предназначенные для борьбы с ВИЧ-инфекцией, уже
проходят клинические испытания.
ВЛИЯНИЕ НА СПОСОБНОСТЬ БАКТЕРИЙ ПРОНИКАТЬ В КЛЕТКУ-
ХОЗЯИНА
Создание вакцины, которая многократно усиливала бы
иммунный ответ организма. Использование такой вакцины или
антибиотиков вместе с противовоспалительными средствами
могло бы уменьшить наносимый организму вред. Впрочем,
опыты на животных пока не дали положительных результатов.
ПОДАВЛЕНИЕ РАЗМНОЖЕНИЯ БАКТЕРИЙ В ИНФИЦИРОВАННЫХ
КЛЕТКАХ
Снижение функциональной активности белков, которые
использует хламидия для захвата липидов клетки-хозяина
и поглощения питательных веществ из цитоплазмы. Когда
такие белки будут идентифицированы, их можно будет
выводить из строя с помощью специальных вакцин.
НАРУШЕНИЕ ФУНКЦИЙ БАКТЕРИЙ, НАХОДЯЩИХСЯ ВНУТРИ
КЛЕТКИ
Выведение из строя системы секреции типа III,
высвобождающей белки, которые отражают атаку лизосом,
клеточных органелл, уничтожающих чужаков.
Опыты in vitro показывают, что бактерии с почти такими же
устройствами не вызывали инфекции после инактивации
генов, которые кодируют белковые компоненты устройств.
ЛИШЕНИЕ БАКТЕРИЙ СПОСОБНОСТИ К РАСПРОСТРАНЕНИЮ
Провоцирование самоуничтожения инфицированных клеток
до перехода бактерий в состояние, при котором они могут
заражать другие клетки. Здесь можно сослаться на работы
по созданию веществ, вызывающих преждевременную
гибель опухолевых клеток. Возможно, такие же вещества
можно будет использовать и для уничтожения клеток,
инфицированных хламидиями.
|
убить приютившую их клетку и выйти во внеклеточную среду таким
способом, который минимизирует вероятность обнаружения этого события иммунной системой организма. В результате инфекция свободно
распространяется по всему телу. Чтобы прояснить детали последней стадии жизненного цикла бактерии, нужно продолжить исследование белков, участвующих в инициации апоптоза и блокирующих поступление сигнала к апоптозу хронически инфицированным клеткам. Можно предположить, что второй путь более перспективен с точки зрения создания вакцин. Если
устранить препятствия к переходу клеток на путь апоптоза, можно будет уничтожить находящиеся в них спящие бактерии и не допустить развития хронической инфекции.
Будущая вакцина против хламидиоза должна вызывать более мощную реакцию обеих компонент иммунной системы, чем сам организм, и при
этом не инициировать длительный воспалительный процесс. Что касается хламидиозов, передающихся половым путем, то здесь есть еще одна
проблема: нужно добиться того, чтобы клетки памяти оставались в тканях
мочеполовой системы, готовые в любое время вступить в бой с инфекцией. Дело в том, что в мочеполовом тракте нет тканей, где образовывались
бы клетки памяти. После вакцинации организм остается невосприимчивым
к инфекции лишь в течение того непродолжительного времени, пока эти
клетки находятся в тканях.
От последствий хламидиоза особенно страдают женщины, поэтому
одним из самых серьезных побудительных мотивов к созданию вакцины служит защита женщин от сопутствующих заболеваний. Однако следует вакцинировать не только женщин, но и мужчин. Вакцина в этом случае должна стимулировать образование антител в количестве, достаточном только для уменьшения уровня патогена в организме, а не для полного его уничтожения. Тогда, если женщина заразится от мужчины во время полового акта, клеток памяти, образовавшихся в ее организме в результате вакцинации, будет достаточно для устранения относительно небольшого числа хламидий еще до того, как они дойдут до фаллопиевых труб. Пока вакцина не создана, можно пользоваться таким достаточно эффективным средством, как контрацептивы, содержащие
противохламидиозные препараты. Это могут быть агенты, либо блокирующие присоединение хламидий к клеткам слизистой мочеполового
тракта, либо действующие на белки, которые секретируют микроорга-
низмы для поддержания своей выживаемости вне клеток. Что же касается
трахомы и других болезней, то здесь полно стью предотвратить инфекцию
сможет только вакцинация.
Не следует забывать и о таком давно известном средстве борьбы
с хламидиозами, как антибиотики. К счастью, геном Chlamydia за миллионы лет практически не изменился. Это означает, что данный микроорганизм неохотно включает в свой геном новые гены, в том числе и гены
устойчивости к антибиотикам. Однако антибиотики не могут устранить те повреждения в тканях, которые возникли в результате воспаления, а кроме того, они эффективны только на ранних стадиях заболевания. Поэтому проблема массового обследования людей, относящихся к группе риска, остается. Уже доказана результативность такого неинвазивного метода, как анализ мочи сексуально активных молодых людей обоего пола. Однако все эти меры никоим образом не подменяют собой работы
по созданию эффективных вакцин.


