|
Гэри Стикс январь 2005 № 1 "В МИРЕ НАУКИ" | |||
|
Полным
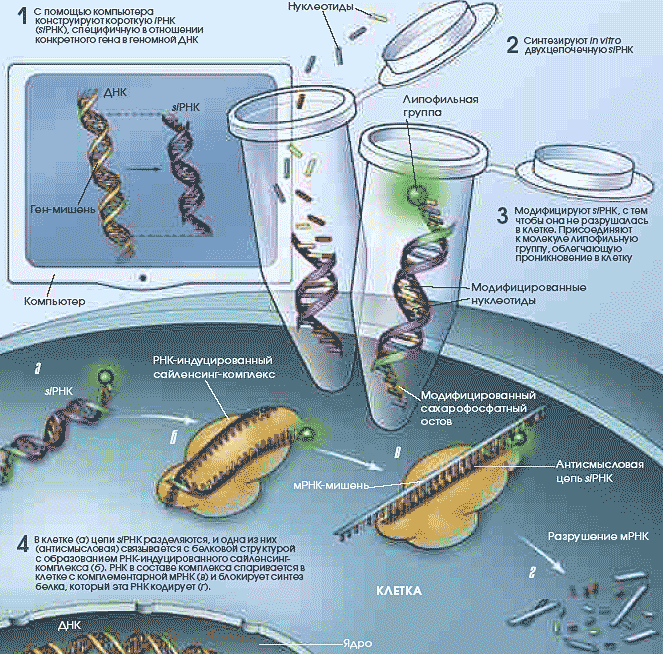
ходом идут работы по созданию совершенно новых лекарственных препаратов, прицельно выводящих из строя РНК.
| В 1996 г. журнал Worth сообщил, что вскоре мы станем свидетелями появления еще одного гиганта масштабов Microsoft, и это будет компания
Isis Pharmaceuticals. Надо отдать должное, Isis – один из лидеров в так называемой антисмысловой биотехнологии. Но путь к применению
этой методики для лечения онкологических и других заболеваний
усеян осколками разбившихся надежд.И вот недавно появилась многообещающая технология блокирования генов. «В течение четверти века в заявках на получение грантов я писал, что последующие пять лет собираюсь посвятить созданию нового метода инактивации
генов в клетках млекопитающих in vitro, – говорит Филип Шарп (Phillip A. Sharp), директор Института Макговерна по исследованию
мозга при Массачусетском технологическом институте. – Но всякий раз новый способ оказывался настолько неуклюжим и нелепым,
что его практическое применение было нереально».
Сегодня все внимание Шарпа, получившего в 1993 г. Нобелевскую премию по физиологии и медицине, приковано к недавнему открытию.
Оно состоит в том, что у клеток есть неизвестный прежде механизм блокирования экспрессии генов – РНК-интерференция (РНКi). Блокирование происходит на уровне трансляции – синтеза белка на кодирующей его мРНК. Механизм вступает в действие, например, в тот момент, когда вирус, инфицировавший клетку, пытается переключить белок-синтезирующий
аппарат хозяина на образование вирусных белков.В 1998 г. Эндрю Файер (Andrew Z. Fire) из медицинской школы Стэнфордского университета и Крейг Мелло (Craig C. Mello) из Массачусетского университета обнаружили,
что введение круглому червю небольших количеств двухцепочечной
РНК (дцРНК), кодируемой определенным геном, полностью выключает экспрессию последнего. А в 2001 г. Томас Тушл (Thomas Tuschl) из Рокфеллеровского университета показал, что укороченные
версии дцРНК (siРНК, от англ. short interfering RNA) заставляют «замолчать» гены-мишени в клетках млекопитающих в культуре. И даже если надежды ученых на применение новой методики не оправдаются, совершенно очевидно, что некоторых ее создателей ожидает высшая научная награда – Нобелевская премия. «Открытие феномена РНК-интерференции
чрезвычайно важно не только для медицины, но и для биологии
в целом», – замечает Шарп (см. «Геномные цензоры», «В мире науки», №11, 2003 г.).
Но насколько siРНК отличаются от антисмысловых РНК? На первый
взгляд различие невелико. Антисмысловые РНК – это полинуклеотидные
цепочки, полученные искусственным путем. Они связываются
с мРНК, которые содержат комплементарные им последовательности,
что приводит к блокированию экспрессии соответствующих
генов. siРНК тоже заставляет ген замолчать и использует для этого комплементарное спаривание с РНК. Происходит это следующим образом: в клетке siРНК переходит в одноцепочечную форму, и одна из цепей (антисмысловая) включается в состав белкового комплекса, в результате – образуется РНК-индуцированный сайленсинг-комплекс (RISC, от англ. RNA-induced silencing complex). RISC связывается с мРНК, комплементарной антисмысловой цепи в составе комплекса, и особый фермент разрезает мРНК.Однако в отличие от антисмысловых
РНК, которыми ученые занимались последние 15 лет, siРНК – инструмент многоразового использования. Они связываются все с новыми и новыми молекулами специфической мРНК, каждый раз выводя их из строя. «Потенциал siРНК в 100, а то и в 1000 раз больше, чем у антисмысловых РНК», – говорит Джуди Либерман (Judy Lieberman), ведущий специалист Института биомедицинских исследований в Бостоне.
Сегодня с siРНК-технологиями связана деятельность более 100 компаний. Половина из них занимается поставкой на рынок химикатов и новых технологий, необходимых для исследований в этой области, другие проводят эксперименты с siРНК на коммерческой основе. Небольшая часть фирм сосредоточилась на медицин-ских аспектах siРНК-технологий. В создании одной из них в 2002 г. принимали участие отцы-основатели
новой отрасли Тушл, Шарп и Дэвид Бартел (David P. Bartel) из Массачусетского технологического института. Речь идет об Alnylam Pharmaceuticals (в переводе с арабского Alnylam означает «нитка жемчуга
», так называется яркая звезда в созвездии Ориона). На столь экзотическом названии настоял профессор молекулярной биологии
и химии в Исследовательском Океанографическом институте
Скриппса Пол Шиммел (Paul R. Schimmel). По его словам, такое название будет нелегко запомнить, но и сложно забыть.
«Звездная команда» была готова приступить к делу. Но, когда исполнительный директор компании Джон Мараганоре (John M. Maraganore) стал подыскивать людей, которые реально занялись бы созданием siРНК-препаратов, он начал вовсе не с ученых, а с юристов. «Четверо из пяти должны заниматься проблемами интеллектуальной собственности, и только один – наукой», – считает Мараганоре. Он убежден, что финансовый успех зависит от юридических тонкостей не меньше, чем от научных ухищрений. Шумиха, поднятая вокруг РНКi, помогла найти деньги. Сегодня капитализация компании составляет $85 млн. – сумма, достаточная для работы в течение двух лет. За это время предполагается создать препарат и начать его клинические испытания.Успех или неудача во многом зависят
от того, удастся ли доставлять siРНК в клетки-мишени и обеспечивать
их защиту от клеточных ферментов. siРНК должны находиться в клетке достаточно долго, чтобы выполнить свою миссию – найти специфические мРНК и связаться с ними. Те же проблемы возникали
при работе с антисмысловыми РНК. Alnylam сразу же отбросила
 Связывание матричной РНК (длинная цепь с зубьями) с комплементарной РНК в составе белкового комплекса (короткая цепь). Связывание матричной РНК (длинная цепь с зубьями) с комплементарной РНК в составе белкового комплекса (короткая цепь). метод векторной доставки (например, с помощью вирусов), когда фрагмент ДНК вводится не просто в клетку, а в клеточное ядро, и синтезируемая на нем РНК влияет на экспрессию. Проблемы в этом случае возникали с адресностью доставки и с повышенным риском побочных эффектов. Было решено синтезировать двухцепочечные siРНК длиной в 21 нуклеотидную пару in vitro. Причины, по которым выбор пал именно на этот способ, были весьма необычного свойства. Alnylam переманила одного из руководителей администрации фирмы Isis, предложив ему пост вице-президента отдела по разработке препарата. Мараганоре позвонил президенту
Isis и заверил его в намерении сохранять дружественные отношения
с разработчиками «антисмысловых» технологий, и они договорились
о сотрудничестве. Alnylam должна была заплатить Isis $5 млн. за использование запатентованных ею химических методов доставки и стабилизации РНК. Isis, в свою очередь, инвестировала в Alnylam
$10 млн., тем самым гарантировав себе получение прибыли от продаж siРНК-продуктов.Стратегия разработки siРНК-препаратов в общих чертах повторяет ту, что использовалась создателями «антисмысловых» продуктов. Единственным средством такого рода, получившим одобрение FDA, стал витравен (vitravene) компании Isis, предназначенный для лечения заболевания глаз, от которого страдают ВИЧ-инфицированные. Лекарство инъецируют непосред-ственно в глаз, так что активное вещество концентрируется в нужном месте и не воздействует на другие органы и ткани. Однако рынок сбыта для витравена исчез, поскольку появились методы борьбы с цитомегаловирусной инфекцией (она и была причиной поражения сетчатки у ВИЧ-больных). Возможно, со временем короткие РНК можно будет вводить в кровоток и лечить системные заболевания. Но пока события развиваются
по старому сценарию: в августе заявку на проведение клинических испытаний направила фирма Acuity Pharmaceuticals из Филадельфии, которая
занимается разработкой препарата, предназначенного для лечения
возрастной макулодистрофии.С заявкой в FDA собирается обратиться
также Sirna Therapeutics из Колорадо, и произойдет это на полгода раньше, чем это сделает Alnylam.
| ||